
インフルエンザ治療薬アビガンがコロナウイルスに効くというのが話題になっていますね!
もとは富山化学のお薬ですが、現在は富士フイルムが富山化学を買収していますので、富士フイルムのお薬ですね。
そんなわけで、富士フイルムはストップ高からの木曜日は大きく下げるという、一人ジェットコースターをしていました。
まるで特効薬のようにもてはやされていますが、現実はどうなのでしょうか。
作用機序や有効性、副作用等から考えてみましょう。
Contents
要約
・富士フイルムのアビガンは対インフルエンザの切り札
・アビガンは通常の条件では使用できないお薬(流通していない)
・アビガンは催奇形性の副作用が強く、ぽんぽこ使用できる薬ではない
・データベースから実施中の臨床試験を2試験確認
・アビガンで全て解決とはいかない!
アビガン(ファビピラビル)とは?
アビガンはインフルエンザ治療薬として承認はされているものの、一般に流通しているお薬ではありません。
この薬はノイラミニダーゼ阻害薬(タミフル・イナビルのような普通のインフルエンザ治療薬)が効かないインフルエンザウイルスに感染した患者さん用のスーパーインフルエンザ治療薬なのです。
なぜ市場に流通していないのかを説明する前に、作用機序や副作用を見ていきましょう。
アビガンの作用機序
アビガンは体内で代謝されて活性体となります。
その活性体がRNAポリメラーゼを阻害することで、ウイルスの増殖を防ぐとされています。
RNAはいわばウイルスの設計図。
ポリメラーゼはその設計図を複製する酵素です。
この薬はウイルスを駆逐するというよりかは、増殖を防ぐ薬ということですね。
・・・この文章に見覚えがありますか?
そうです。
先日ご紹介したギリアドのレムデシビルとおおもとの原理は同じです。
なおタミフル達はノイラミニダーゼの阻害が作用機序ですが、これはウイルスが細胞から出ていくことを阻害するという機序になります。
同じインフルエンザ治療薬でも、作用機序は異なるのですね。
インフルエンザ治療薬の作用機序を図としてまとめておきます。
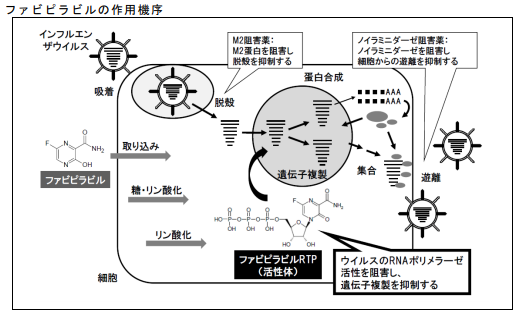
副作用
承認用法及び用量における投与経験はありません。
国内臨床試験及び国際共同第Ⅲ相試験(承認用法及び用量より低用量で実施された試験)においては501例中副作用が100 (19.96%)に認められています。
主な副作用は血中尿酸増加24例(4.79%)、下痢24例(4.79%)等です。
大した事なく見えますよね?
実際この用量でこの副作用は大したことないのですが、クリティカルな副作用が別にあります。
動物実験において、初期胚が上手く形成されなかったり催奇形性が確認されているのです!
そのため妊婦又は妊娠している可能性のある婦人には投与しないこと(禁忌)とされています。
また女性だけ注意すればよいわけではありません。
この薬は精液中へも移行するのです。
つまり男性も避妊が必要になるということです。
この作用ですがRNA複製阻害を行う際に、ウイルスだけではなく、ヒトの細胞でも同じように阻害してしまうことがあるので、この副作用が出るのですね。
このような事情もあり、もしこのお薬を使わなければならない場合は、「治療開始に先立ち、患者又はその家族等に有効性及び危険性(胎児への曝露の危険性を含む) を十分に文書にて説明し、文書で同意を得てから投与を開始する」とされています。
なかなか大仰なお薬であることがお分かりいただけたでしょうか。
使用の条件
「アビガンは、新型又は再興型インフルエンザウイルス感染症が発生し、本剤を当該
インフルエンザウイルスへの対策に使用すると国が判断した場合にのみ、患者への
投与が検討される医薬品であり、厚生労働大臣からの要請を受けて製造販売を行う。」
医薬品インタビューフォームには上記のように記載されています。
そのため、アビガンはトリインフルエンザ等の新型インフルエンザが流行したときにのみ使用する最後の砦となるお薬というわけです。
なお国が200万人分を備蓄しており在庫は十分ということです。
つまり富士フイルムがぼろ儲けできる下地はありません。
コロナウイルス(COVID-19)に対する臨床試験
さて、では実際に行われている臨床試験について見てみましょう。
いつも通りClinicalTrials.gov(アメリカ:NIH)で検索してみました。
このデータベースは、NIHの運営している臨床試験を集約した最大のデータベースであり、世界200カ国以上の国から30万件以上の臨床試験が登録されています。
「COVID-19,Favipiravir」で検索したところ、2試験見つかりました。
Favipiravir Combined With Tocilizumab in the Treatment of Corona Virus Disease 2019
2020年3月からスタートした治験で、2020年5月までに終了予定です。
患者数は150人予定。
トシリズマブ(アクテムラ:中外製薬)との併用試験みたいですね。
この試験が上手くいったら、今度は中外が噴き上げたりして(笑)
https://clinicaltrials.gov/ct2/show/NCT04310228?cond=COVID-19+Favipiravir&draw=2&rank=1
Various Combination of Protease Inhibitors, Oseltamivir, Favipiravir, and Chloroquin for Treatment of COVID19 : A Randomized Control Trial
2020年3月からスタートしたP3試験で、2020年11月までに終了予定です。
患者数は80人予定。
オセルタミビル(タミフル:中外)やリトナビル(カレトラやヴィキラックス)等も使用する試験です。
https://clinicaltrials.gov/ct2/show/NCT04303299?cond=COVID-19+Favipiravir&draw=2&rank=2
日本でも臨床研究段階ですが、群馬大等が動いているようです!
なお17日に中国政府は自国内で行った320例の臨床研究にて、アビガンの新型コロナウイルスへの有効性が確認されたと発表しています。
中国だけの臨床研究という、何とも言えない感じですが、作用機序的に、まぁ効かないことはないよねーといった印象です。
副作用もないとのことで、怪しさ満点ですね(笑)
本当なの?
今後の展開
このお薬の特性を踏まえると、軽症の患者にどんどん使うのではなく、重症でまずそうな患者に対して、うーんこれしかない!という感じで投与することで、それ以上の悪化を防ぐような使い方となるのではないでしょうか。
軽症段階でぽんぽこ使える感じにはならないと思います。
つまり、アビガンで全て解決とは到底いかないのです。
そして当然アビガンの売れ行きには関係なく、富士フイルムの業績にも影響しないでしょう。
中国での特許切れというそれ以前の問題もあります。
日本では一応2024年までは物質特許は有効ですので、直近で適応を取ればまだ儲かります。
そんなわけで富士フイルムの株価もすぐに元通りになるのではないかと踏んでいます。
というかこの記事上げる時点でだいぶ戻してきていますね。
どこかで書きましたが、「バイオは噴き上げたら売る」がマイルールです。
市場が混乱しているうちに売り抜けましょう。
そうはいっても、COVID-19に対して有効なお薬が少しでも増えることは有意義なことですね。
アビガンは特効薬とはいきませんが、他の薬やワクチンができるまでのつなぎとしては十分な役割を担えるのではないかと思います!







